Química -
Como acelerar a reação que transforma o estudante do ensino médio em universitário?
Considere entrar na universidade como sendo resultado da seguinte reação química:
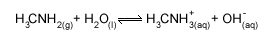
Saiba agora quais os fatores que podem acelerar essa reação:
Podemos admitir que o vestibular nesta reação funciona como o catalisador que acelera a reação, sem interferir no produto final.
Aumentando a concentração do estudante, ou melhor, a concentração dos reagentes, também conseguimos acelerar a reação (Lei de Guldberg-Waage).
Quanto mais intimidade o aluno tiver com a prova, maior a rapidez da reação. Se um dos reagentes for sólido, quanto mais particulado (pó), maior será a área de contato. Isso acelera a reação.
Quanto mais quente, mais rápida a transformação. Conforme o sistema reagente é aquecido, maior é a energia cinética molecular, aumentando o número de choques efetivos e a rapidez da reação.
Qual estudante de ensino médio presta vestibular e não fica sob pressão? Difícil.
A pressão acelera a reação por causa da vontade que o candidato tem de ser universitário. Quanto maior a pressão, menor é o volume, maior é o número de choques efetivos e, conseqüentemente, mais acelerada fica a reação. *Perseu Lúcio Alexander Helene de Paula é professor de química desde 1985.Solu








ID: {{comments.info.id}}
URL: {{comments.info.url}}
Ocorreu um erro ao carregar os comentários.
Por favor, tente novamente mais tarde.
{{comments.total}} Comentário
{{comments.total}} Comentários
Seja o primeiro a comentar
Essa discussão está encerrada
Não é possivel enviar novos comentários.
Essa área é exclusiva para você, assinante, ler e comentar.
Só assinantes do UOL podem comentar
Ainda não é assinante? Assine já.
Se você já é assinante do UOL, faça seu login.
O autor da mensagem, e não o UOL, é o responsável pelo comentário. Reserve um tempo para ler as Regras de Uso para comentários.